Introducción
La fabricación continua (FC) de productos farmacéuticos se está convirtiendo gradualmente en un nuevo estándar tecnológico en la industria farmacéutica. Actualmente, la mayoría de los productos farmacéuticos se fabrican mediante un método conocido como fabricación por lotes en el que diferentes operaciones, como el pesaje, la mezcla, la formación de tabletas o el encapsulado, se realizan separadamente y en momentos diferentes. Este es un proceso largo de varios pasos que requiere equipos a gran escala. La FC es más rápida que el procesamiento por lotes y más fácil de escalar. Elimina la necesidad de detener y mover productos intermedios entre los pasos de producción, lo que puede mejorar potencialmente la calidad del producto farmacéutico final.1,2
En este estudio, se investigó la viabilidad de una granulación de doble tornillo para la producción continua de comprimidos liqui-sólidos de simeticona y clorhidrato de loperamida. La simeticona es una mezcla de polidimetilsiloxano y dióxido de silicio que se usa comúnmente como agente antiespumígeno para aliviar las molestias abdominales causadas por el exceso de gases intestinales. La loperamida es un fármaco antidiarreico eficaz que se administra ampliamente para el tratamiento sintomático de varios tipos de diarrea. Las combinaciones de dosis fijas que contienen 2 mg de clorhidrato de loperamida y 125 mg de simeticona ya se encuentran disponibles en el mercado.3,4
Materiales
Simeticona Q7-2243 LVA de Dow Corning GmbH (Wiesbaden, Alemania). Clorhidrato de loperamida de Vasudha Pharma Chem Limited (Hyderabad, India). Fosfato de calcio tribásico (TRI-CAFOS® 500) y fosfato de calcio dibásico (DI-CAFOS® A150) de Chemische Fabrik Budenheim KG (Budenheim, Alemania). Croscaramelosa de sodio (Ac-Di-Sol® SD-711 NF) de FMC BioPolymer (Filadelfia, Estados Unidos) y estearato de magnesio (Ligamed® MF-2-V) de Peter Greven Fett-Chemie (Venlo, Países Bajos).
Métodos
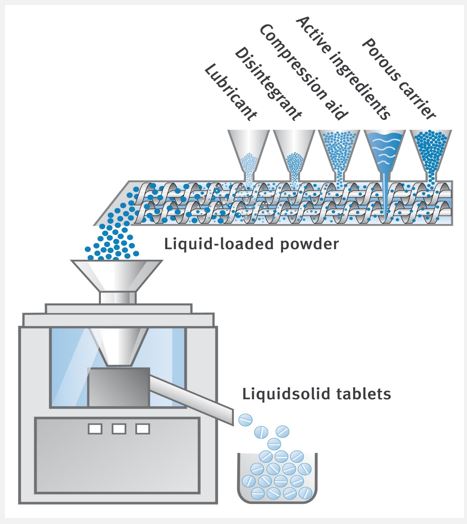
Una mezcla para comprimidos que contiene 16,96 % de simeticona y 0,27 % de clorhidrato de loperamida como ingredientes activos, 50,90 % de TRI-CAFOS® 500 (portador poroso), 29,87 % de DI-CAFOS® A150 (auxiliar de compresión), 1,00 % de Ac-Di -Sol® SD-711 NF (desintegrante) y 1,00 % de Ligamed® MF-2-V (lubricante) se procesó con un extrusor de doble tornillo Thermo Scientific™ Pharma 16 (Thermo Electron GmbH, Karlsruhe, Alemania) configurado para que todos los ingredientes se dosificaran de forma simultánea y continua. La extrusora se hizo funcionar a una velocidad de tornillo de 400 rpm y un rendimiento total de 10 kg/h. Los polvos obtenidos se comprimieron directamente con una prensa rotatoria Fette 102i (Fette Compacting GmbH, Schwarzenbek, Alemania) operada a una velocidad de 62,5 rpm. Se utilizaron punzones redondos de 12 mm, plano y borde biselado con línea de rotura (Fette Compacting GmbH, Schwarzenbek, Alemania). Para caracterizar las propiedades de compresibilidad, se comprimió bajo fuerzas de compactación crecientes de 10, 15, 20 y 25 kN (equivalentes a 87, 130, 174 y 217 MPa respectivamente) con una precompresión del 10%. Un diagrama esquemático del conjunto de equipos utilizados en este estudio se muestra en la Figura 1.
Resultados y Discusión
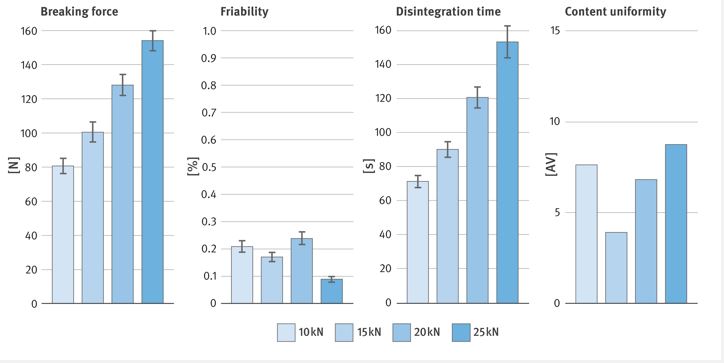
En este estudio se prepararon comprimidos liqui-sólidos de simeticona y clorhidrato de loperamida. Ambos principios activos suponían un gran reto tecnológico, ya que la simeticona era una sustancia líquida y oleosa, y en la formulación se utilizaba clorhidrato de loperamida en una cantidad mínima. La Figura 2 muestra una comparación de las propiedades seleccionadas de las tabletas liqui-sólidas desarrolladas en este trabajo, comprimidas bajo diferentes fuerzas de compresión (las columnas subsiguientes representan fuerzas de compresión crecientes). Todas las pruebas se llevaron a cabo de acuerdo con las monografías de farmacopea pertinentes. La uniformidad de dosis se probó mediante la prueba de Uniformidad de contenido para el clorhidrato de loperamida, ya que está presente en las tabletas en una cantidad muy pequeña (0,27%) y se identificó como el ingrediente más crítico en este sentido.
La formulación desarrollada aquí se caracterizó por su muy buena compresibilidad. Se encontró que la dureza de las tabletas, expresada como fuerza de rotura, era satisfactoria incluso a una fuerza de compresión relativamente baja de 10 kN. Esta propiedad mejoró gradualmente con el aumento de la fuerza de compresión. Se pudo observar una relación similar en el caso del tiempo de desintegración. Sin embargo, incluso para la fuerza de compresión más alta de 25 kN, el tiempo de desintegración fue muy corto y no superó los 3 minutos. Los comprimidos se caracterizaron por una friabilidad muy baja y una uniformidad de contenido adecuada (los valores de aceptación AV estaban muy por debajo del límite requerido de 15) independientemente de la fuerza de compresión aplicada. Los resultados obtenidos demostraron que el método elegido para preparar la mezcla de polvo con la ayuda de un granulador de doble tornillo evidenció propiedades que permitieron una exitosa compresión de tabletas.
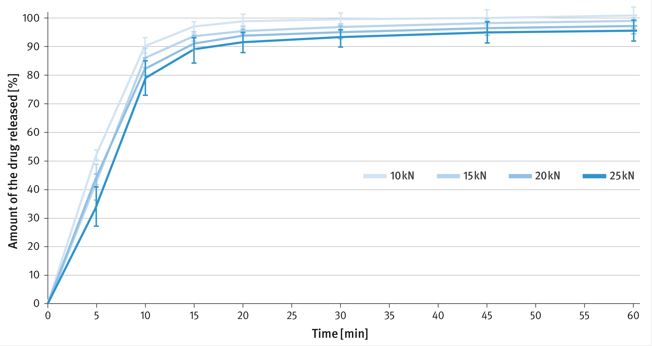
La prueba de disolución se llevó a cabo solo para el componente crítico en 900 mL de HCl 0,1 M usando un aparato USP I (canastas) PTWS 820D (Pharma Test Apparatebau AG, Hainburg, Alemania) operado a 100 rpm y temperatura de 37 ˚C. En la Figura 3 se muestra una comparación de los perfiles de disolución de tabletas comprimidas bajo diferentes fuerzas de compresión. Todas las tabletas liberaron el fármaco muy rápidamente, de modo que en los primeros 15 minutos de la prueba se disolvió más del 85 % del clorhidrato de loperamida.
Los perfiles de disolución de diferentes fuerzas de compresión fueron similares. No se observó un efecto significativo de la fuerza de compresión aplicada o tampoco de la dureza alcanzada en la tasa de disolución de la sustancia farmacológica.
Conclusiones
A lo largo del estudio presentado se desarrollaron con éxito comprimidos liqui-sólidos de 125 mg de simeticona y 2 mg de clorhidrato de loperamida. Aunque el proceso de producción se llevó a cabo a pequeña escala, el diseño del equipo simuló una línea de producción continua. El estudio demostró que el uso de un granulador de doble tornillo permitió realizar eficientemente la deposición de simeticona sobre un portador poroso (TRI-CAFOS® 500), que al mismo tiempo proporcionó una adecuada uniformidad de contenido, como se evidenció con el componente más crítico de la formulación – clorhidrato de loperamida.
Referencias
Lee, S.L. Modernizing the Way Drugs Are Made: A Transition to Continuous Manufacturing (2017), www.fda.gov/drugs/news-events-human-drugs/modernizing-way-drugs-are-made-transition-continuous-manufacturing;
Wahlich, J. Review: Continuous Manufacturing of Small Molecule Solid Oral Dosage Forms. Pharmaceutics, 13, 1311 (2021);
Kaplan, M.A. et al. Loperamide-simethicone vs loperamide alone, simethicone alone, and placebo in the treatment of acute diarrhea with gas-related abdominal discomfort. A randomized controlled trial. Arch Fam Med. 8, 243-248 (1999);
McNeil Products Ltd. SmPC: Imodium Dual Action Relief Tablets (P) (2021), www.medicines.org.uk/emc/product/370/smpc#gref.